

Le charançon de la betterave, Lixus juncii est un coléoptère de la famille des Curculionidae. Cet insecte polyphage peut se nourrir de nombreuses espèces de plantes, notamment de la famille des Amaranthacées, dont fait partie la betterave. Les larves de ce ravageur peuvent occasionner des dégâts dans les cultures de betteraves, de blettes et d'épinards.
Dernière mise à jour : avril 2026
Le cycle de vie du charançon se compose de 3 stades larvaires, d’un stade nymphal et d’un stade adulte. Les stades larvaire et nymphal se déroulent au sein de la betterave, dans les pétioles, les tiges ou la racine. La durée des différents stades et le nombre de générations annuelles varient selon la zone géographique. Dans les régions tempérées comme la France, environ 60 jours sont nécessaires pour passer d’un œuf au stade adulte, alors qu’il faut uniquement 45 jours au Maroc, par exemple. Le charançon peut ainsi développer 2 générations successives par an dans les pays du sud de la Méditerranée, tandis qu'il n’en a qu’une dans les pays européens.
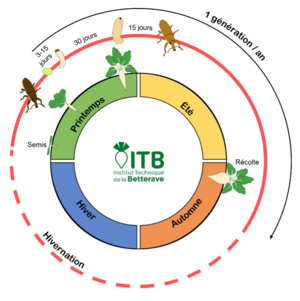
Les charançons vivent environ 1 an. Ils colonisent les parcelles de betteraves au printemps, entre fin avril et début mai en fonction des années et des régions, où ils vont se nourrir des feuilles. Les accouplements semblent débuter avant l’arrivée des individus en parcelle de betteraves (Coussy, 2025). Quelques jours après leur arrivée dans les parcelles, les femelles commencent à pondre leurs œufs dans les pétioles même lorsque les betteraves sont encore jeunes (4-6 feuilles). La femelle creuse un trou dans les pétioles à l’aide de son rostre. Elle dépose un œuf par trou qu’elle rebouche ensuite avec un liquide buccal protecteur (Ocete et al., 1994). Une femelle peut pondre une dizaine d’œufs par jour, pour un total de 100 à 350 œufs dans sa vie (Lebouc, 2003). Les accouplements et les pontes se poursuivent jusqu’à la fin de vie des individus vers fin juin, début juillet. À la suite de l’éclosion, 3 à 15 jours après la ponte, la larve se développe dans les tissus où elle creuse une galerie en se nourrissant. En fonction des conditions environnementales, elle peut descendre vers le collet et jusqu’à la racine. La nymphose puis l’apparition de l’imago a lieu dans la betterave (Ocete et al., 1994 ; Lebouc, 2003). La nouvelle génération d’adultes émerge des betteraves courant juillet et se nourrit du feuillage de la plante hôte, les deux générations se côtoient donc un court laps de temps. Ces individus émergents sont incapables de s’accoupler car l’appareil reproducteur des femelles n’est pas développé. Ils quittent alors les parcelles de betteraves à la recherche d’un lieu pour passer l’hiver.
Plusieurs points restent à éclaircir concernant le cycle de vie du charançon. Comme indiqué précédemment, les individus de la nouvelle génération sont incapables de se reproduire dans les semaines qui suivent leur émergence en été. Cependant, la période de développement de l’appareil reproducteur des femelles n’est pas encore identifiée. Les données de captures montrent que les premières femelles trouvées dans les parcelles de betteraves n’ont pas toutes atteint la maturité sexuelle. Un déclenchement de la maturation de l’appareil reproducteur lors de la reprise de l’activité à la sortie de l’hiver pourrait expliquer cette observation. Toutefois des expériences plus approfondies sont nécessaires pour valider cette hypothèse et préciser les facteurs qui déclenchent cette maturation. De plus, parmi ces premières femelles, toutes ne sont pas accouplées, ce qui interroge sur le moment de la reproduction. Ces deux éléments représentent un enjeu important pour le développement d’une stratégie de lutte basée sur la confusion sexuelle ou l’attraction via des phéromones. En effet, son efficacité serait moindre si les femelles sont fécondées avant leur arrivée dans les parcelles.
Des recherches sont également à mener pour identifier les sites d’hivernation du charançon, les dernières études n’ayant pas permis de les localiser (Coussy, 2025). Cette connaissance permettra de mieux comprendre les dynamiques de colonisation des parcelles et, ainsi, d’identifier précocement les zones à risque. Il sera donc possible d’intervenir dans ces lieux pendant l’hiver, lorsque les individus sont vulnérables, afin de limiter les populations.
Originaire d’Europe, ce ravageur a d’abord causé des dégâts dans les cultures de betteraves porte-graine dans le sud de la France avant les années 2000. Son passage vers les cultures de betteraves sucrières est beaucoup plus récent, les premiers dégâts ont été signalés dans les plaines de Limagne à partir de 2010. Il a ensuite progressé d’année en année en s’implantant successivement dans la région Centre en 2015, puis dans le sud de l’Ile-de-France, l’Yonne et l’Aube en 2018 avant d’atteindre le sud des Hauts-de-France en 2020. Si la majorité des régions au sud de Paris sont touchées, la pression du ravageur varie entre les départements et d’une année sur l’autre.
Depuis 2022, l’ITB met à disposition un outil interactif, Alerte Charançons, qui permet de visualiser en temps réel la présence du charançon, à l’échelle du territoire. Ces données proviennent de Vigicultures© qui mobilise un vaste réseau de parcelles de betteraves sucrières et de betteraves porte-graines. Des notations hebdomadaires y sont réalisées dans les différentes zones de production pour suivre l’évolution des bioagresseurs durant la saison. L’OAD Alerte Charançons intègre aussi un modèle qui indique si les températures observées depuis le début de l’année sont propices à l’arrivée du ravageur, quelle que soit la localisation en France. Cet outil est accessible via la rubrique « Outils » du site web de l’ITB ou sur http://charancons.itbfr.org/.
La régulation des ravageurs par les ennemis naturels n’est pas toujours simple à attester, car cela nécessite d’observer la prédation ou le parasitisme directement ou via les traces qu’ils laissent. Ces interactions peuvent avoir lieu aux différents stades de vie du ravageur, qu’il vive dans la plante ou libre dans l’environnement.
Chez L. juncii, les observations sur le terrain révèlent quelques événements de prédation des individus au stade adulte, notamment par des araignées.

L. juncii adulte capturé par une araignée
Le stade larvaire est également sujet à la régulation naturelle. En effet, plusieurs espèces d’hyménoptères parasitoïdes ont été identifiées comme des auxiliaires de L. juncii. Durant l’été 2022, l’ITB a mené une campagne d’échantillonnage des parasitoïdes du charançon après avoir constaté leur forte prévalence dans plusieurs parcelles touchées par le ravageur. Effectivement, 31 % des larves de charançons étaient tuées par un parasitoïde. Cinq espèces ont pu être identifiées à partir des individus trouvés dans les galeries de charançons, avec une espèce principale : Bracon intercessor. Cependant, plusieurs indices sur le terrain semblent indiquer une diversité plus importante d’ennemis naturels, avec notamment des prédateurs ou des parasitoïdes s’attaquant aux œufs du charançon. Une étude a estimé à 70 % la proportion d’œufs qui n’écloront pas, car ils seront détruits par des prédateurs naturels (Duckert, 2025). Il n’existe pas d’études sur les pratiques agricoles qui pourraient être favorables à la présence des différents auxiliaires identifiés.

Parasitoïdes s'attaquant aux larves de L. juncii, au stade nymphe, libre ou dans un cocon (photos au-dessus), et au stade adulte (photos en-dessousen dessous)

Trous de ponte de L. juncii percés d’un trou de prédateur ou de parasitoïde d’œuf
L’adulte mesure entre 9 et 15 mm et présente un corps allongé. Ses pièces buccales forment un rostre, dont la forme est caractéristique des charançons. La couleur du corps varie entre l’orange et le brun foncé mais toujours avec une bande blanche nette et continue sur les flancs, qui part de la tête jusqu’à l’extrémité des élytres. La couleur orange de certains individus s’explique par la présence d’une fine couche poudreuse. Cette couleur est caractéristique des adultes fraîchement émergés, qui deviennent rapidement plus foncés car la poudre responsable de la teinte orangée se détache très facilement du corps sous l’effet de contraintes physiques.

L. juncii adulte
Jeunes adultes de L. juncii. Individus recouverts d’une couche orangée (A et B) et individu bicolore suite à un contact dans les doigts (C)
L’observation des adultes peut être difficile lorsque la pression est faible car ils se laissent aisément tomber au sol dès qu’ils perçoivent un danger. Ils se trouvent le plus souvent sur le haut des feuilles ou au niveau du collet. Des pièges à phéromones sont en cours de test par la filière porte-graine ainsi que par l’ITB afin d’améliorer la détection des adultes dans les parcelles.
Il est possible de distinguer le mâle de la femelle en s’appuyant sur plusieurs critères. Le critère le plus évident reste la position des individus lors de l’accouplement, le mâle se trouvant toujours sur le dos de la femelle. Deux critères morphologiques peuvent toutefois être utilisés pour sexer à la loupe des individus isolés : la forme du dernier segment abdominal et la taille du rostre. Le critère le plus discriminant est l’observation en vue dorsale du dernier segment abdominal situé sous les élytres. Celui des femelles a une forme qui épouse celle des élytres, tandis que celui des mâles est plus large et rectangulaire (Loiseau et Chapelin-Viscardi, 2023). La pilosité de cette zone diffère également selon le sexe, elle est homogène chez les femelles et se poursuit sous les élytres alors que chez les mâles les soies sont plus denses et localisées sur l’extrémité du segment. La longueur du rostre peut aussi contribuer à distinguer le sexe des individus. Les femelles présentent un rostre plus allongé que celui des mâles, mais la différence est plus subtile à observer.

Accouplement de L. juncii
L. juncii mâle (à gauche) et femelle (à droite)

L. juncii femelle (en haut) et mâle (en bas)
L’œuf de L. juncii est jaune clair de forme légèrement ovale.
Œufs de L. juncii
La larve est de type vermiforme apode (absence de pattes), de couleur blanche avec une tête foncée bien définie.
Larves de L. juncii
La nymphe est de grande taille, de couleur blanche ou marron selon le moment de la métamorphose. Elle est capable de se déplacer dans la galerie.
Nymphe de L. juncii
Pour pondre leurs œufs, les femelles charançons creusent un trou dans le pétiole de la plante à l’aide de leur rostre et déposent un œuf unique dans la cavité avant de le reboucher. Par abus de langage, ce trou de ponte est souvent appelé « piqûre ». Les trous de ponte du charançon sont de taille et de forme variables, s’accompagnant le plus souvent d’une boursouflure.

Diversité de forme des trous de ponte de L. juncii
Les trous de ponte ne constituent pas un danger majeur pour la plante. Cependant, c'est un indice important sur le terrain pour détecter l’arrivée du charançon dans une parcelle. Ils constituent un indicateur du niveau d’infestation, notamment en mesurant le pourcentage de plantes touchées et/ou le nombre de trous par plante. Dans les parcelles très touchées, plusieurs dizaines de trous de ponte peuvent se trouver sur la même plante avec plus d’une dizaine de trous par pétiole. Apparemment, les plantes présentant des pétioles plus gros, donc contenant plus de ressources trophiques, seraient préférées des femelles. Elles présenteraient plus de piqûres. Les pertes directes liées aux galeries dans les pétioles et les collets sont seulement de 5 % (Coussy, 2025).
Les principaux dommages sont causés par les larves lorsqu’elles creusent des galeries qui descendent du pétiole jusqu’à la racine. Dans certains cas, les galeries dans le pétiole sont visibles en surface. Cependant, toutes les larves ne migrent pas dans la racine, certaines terminent leur cycle dans le pétiole. Dans les deux cas, le charançon, une fois arrivé au stade adulte, émerge de la betterave en laissant un gros trou derrière lui.

Galeries de L. juncii dans le pétiole (à gauche) et dans la racine (à droite)
Trous d’émergence de L. juncii dans le pétiole (à gauche) et dans la racine (à droite)
Il est important de ne pas confondre les galeries du charançon avec celles que peuvent faire les teignes (pas de trou de ponte pour les teignes).
Trous de ponte de L. juncii (A) et dégâts de teigne (B et C)
Bien que les dégâts du charançon soient similaires qu’ils touchent une betterave sucrière, potagère ou porte-graine, les conséquences diffèrent nettement :
Betteraves sucrières infestées par du Rhizopus suite aux galeries laissées par L. juncii
À ce jour, il n’existe pas de méthode efficace de lutte contre le Lixus juncii mais la recherche est active sur le sujet. Parmi les méthodes explorées on retrouve entre autres l’application de produits, l’utilisation de plantes de service, le recours à des variétés rmoins sensibles :
En 2025, a démarré le projet COLEOFAST (Fédérer et Accompagner la recherche de Solutions Techniques innovantes pour protéger les cultures contre les COLEOptères) qui regroupe notamment les filières betterave porte-graines et betterave sucrière sur le sujet des Lixus. Ce projet permettra de renforcer le suivi des populations dans le but d’améliorer l’outil Alerte Charançons et d’explorer des méthodes de lutte au champ (tolérance variétale, produits de biocontrôle, plantes de services, combinaison de leviers).
Références Agroscope. Info Cultures maraîchères. 2025. Coussy, B.. Ubelix : Utilisation de plantes de service en production de betterave pour gérer les populations de lixus. 2025. Duckert. « Charançon de la betterave (Lixus juncii) : un ravageur favorisé par le réchauffement climatique ? » 2025. Germann, Christoph, et Stève Breitenmoser. Lixus juncii Boheman, 1835 – confirmation de sa présence en Suisse (Coleoptera: Curculionidae). 2020, 4. Lebouc A., 2003 – Mise en place de la lutte raisonnée contre le Lixus de la betterave. Mémoire de fin d’études INP-ENSAT, 39p. Loiseau S., Chapelin-Viscardi J.-D., 2023 - Typologie du développement de l’appareil reproducteur femelle de Lixus juncii Boheman, 1835 (Coleoptera Curculionidae Lixinae). L’Entomologiste, tome 79, 2023, n° 3 : 183 – 193. Ocete, R., et M. E. Ocete. Aproximación a la fenología de Lixus junci Boheman (Coleoptera: Curculionidae) en La Rioja Alta: estimación de las pérdidas que causa. 1994, 6. Rakotoarimanana. Fiche techniques Lixus juncii Charançon de la betterave (et de la blette). 2022. Sochard. Le cahier technique Lixus juncii : résultats des expériences 2023. 2023. Wider. « La betterave sucrière Mise au point ravageurs ». Séances d’informations phytosanitaires, 2024. |
Agrément conseil de l’ITB à l’utilisation des produits phytosanitaires n° 7500002.
Assurance RC n° 05421646Y/1025.
Le portail EcophytoPIC recense les techniques alternatives à l’utilisation des produits phytopharmaceutiques.
Organisme agréé Crédit d'impôt Recherche
L'Institut Technique de la Betterave est
membre du réseau Acta
Institut Technique Agricole Qualifié
par le Ministère de l’Agriculture et de l’Alimentation